Especificidad enzimática.2013
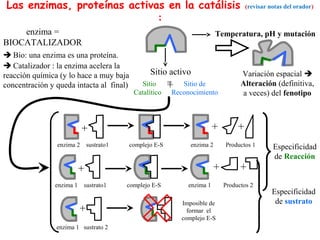
- 1. Las enzimas, proteínas activas en la catálisis (revisar notas del orador) : enzima = Temperatura, pH y mutación BIOCATALIZADOR Bio: una enzima es una proteína. Catalizador : la enzima acelera la reacción química (y lo hace a muy baja Sitio activo Variación espacial concentración y queda intacta al final) Sitio = Sitio de + Alteración (definitiva, Catalítico Reconocimiento a veces) del fenotipo + + + enzima 2 sustrato1 complejo E-S enzima 2 Productos 1 Especificidad de Reacción + + + enzima 1 sustrato1 complejo E-S enzima 1 Productos 2 Especificidad Imposible de de sustrato + formar el complejo E-S enzima 1 sustrato 2
Notas del editor
- RECONOCIMIENTO Y CATÁLISIS Las enzimas presentan dentro de su estructura proteica 2 regiones o sitios importantes para la realización de su actividad catalítica, Sitio de reconocimiento , reconoce y liga al sustrato Sitio catalítico , una vez unido el sustrato, cataliza la reacción Estos 2 sitios están adyacentes uno al otro en la forma activa de la enzima y, en ocasiones, el sitio catalítico es parte del sitio de reconocimiento, Estas 2 regiones en conjunto reciben el nombre de centro o sitio activo de la enzima UNA DE LAS PRINCIPALES CARACTERÍSTICAS DE LAS ENZIMAS ES SU ALTA ESPECIFICIDAD. Las enzimas son especificas para: a) el substrato b) la reacción Ello significa que las enzimas pueden catalizar la transformación de apenas un substrato o una familia de substratos relacionados estructuralmente, catalizando solo una de las posibles reacciones que ese substrato puede experimentar. Cuando la enzima solo puede actuar sobre un tipo de substrato, se dice que la enzima muestra especificidad absoluta para el substrato . Ese es el caso de la deshidrogenasa succínica, que es especifica para el succinato, o la L-glutámico deshidrogenasa, especifica para el glutamato. Si la enzima puede actuar sobre substratos con estructuras muy similares, se dice que la enzima muestra especificidad relativa para el substrato . La L-aminoácido oxidasa, por ejemplo, puede catalizar la oxidación de diferentes aminoácidos de la serie L. Esta característica de algunas enzimas puede ser aprovechada en algunos escenarios clínicos. Por ejemplo, en pacientes intoxicados con metanol, se utiliza etanol en el tratamiento. La enzima puede unirse a cualquiera de los dos alcoholes (especificidad relativa), pero tiene de 10 a 20 veces mas afinidad por el etanol, lo cual favorece la oxidación del etanol por sobre la oxidación del metanol. Evitar la oxidación del metanol para favorecer su eliminación sin ser transformado, es muy importante, ya que la oxidación metabólica del metanol produce metabolitos muy peligrosos para el organismo, como formaldehido y acido fórmico. La especificidad de reacción consiste en que la enzima solo cataliza una de las posibles reacciones que puede seguir un substrato. En el caso del glutamato, por ejemplo, que puede experimentar diferentes transformaciones, se requiere una enzima diferente para cada una de esas transformaciones: Para transformar Glutamato a: Glutamina (Fijación de amoniaco) : se requiere la enzima Glutamina sintetasa GABA (Descarboxilacion): se requiere la enzima Glutamato Descarboxilasa Alfacetoglutarato: se requiere la enzima Glutamato Deshidrogenasa
