Las enzimas
¿Qué son?
 Las enzimas son proteínas complejas formadas por aminoácidos, que se consideran catalizadores, ya que aceleran básicamente todas las reacciones químicas de los seres vivos. Las enzimas tienen un tamaño muy variable. Las cadenas pueden ser desde los 62 aminoácidos hasta 2500.
Las enzimas son proteínas complejas formadas por aminoácidos, que se consideran catalizadores, ya que aceleran básicamente todas las reacciones químicas de los seres vivos. Las enzimas tienen un tamaño muy variable. Las cadenas pueden ser desde los 62 aminoácidos hasta 2500.
Los biocatalizadores no se consumen ni se alteran en la reacción química, pero hacen posible que esta se desarrolle a la velocidad adecuada. Si no existiesen estas enzimas (o biocatalizadores), las reacciones necesitarían muchísima energía de activación y unas temperaturas que el organismo no podría soportar. (Imagen de 123RF, Dominio Público).
¿Cómo actúan?
Las enzimas están formadas por aminoácidos que ayudan a producir las reacciones químicas. Estos son:
- Los aminoácidos estructurales son aquellos que forman la enzima en sí.
- Los aminoácidos de fijación son los que forman enlaces débiles con las sustancias o moléculas a las que la enzima se va a unir.
- Los aminoácidos catalizadores son los que forman enlaces covalentes con estas moléculas, haciendo que se debiliten y favoreciendo que se rompa su estructura, haciendo posible la reacción química.
 Cada enzima está hecha para una función determinada. Las moléculas o sustancias a las que se unen de forma específica se llaman sustratos (suele haber más de un sustrato). Estos sustratos están unidos directamente mediante enlaces débiles (puentes de hidrógeno o enlaces iónicos) con una parte de la enzima llamada centro activo. Es en este centro activo donde la reacción química se produce. (Imagen de la izquierda, Wikipedia, dominio público).
Cada enzima está hecha para una función determinada. Las moléculas o sustancias a las que se unen de forma específica se llaman sustratos (suele haber más de un sustrato). Estos sustratos están unidos directamente mediante enlaces débiles (puentes de hidrógeno o enlaces iónicos) con una parte de la enzima llamada centro activo. Es en este centro activo donde la reacción química se produce. (Imagen de la izquierda, Wikipedia, dominio público).
El centro activo es una parte muy pequeña de la enzima, pero muy importante. Tiene una estructura tridimensional donde hay una cavidad en la que encaja el sustrato. La enzima tiene aminoácidos que atraen a los sustratos y forman enlaces. Se producen las reacciones químicas y una vez finalizadas, los enlaces se rompen y los productos se liberan. (Imagen de la derecha, biologia-geologia.com, dominio público).
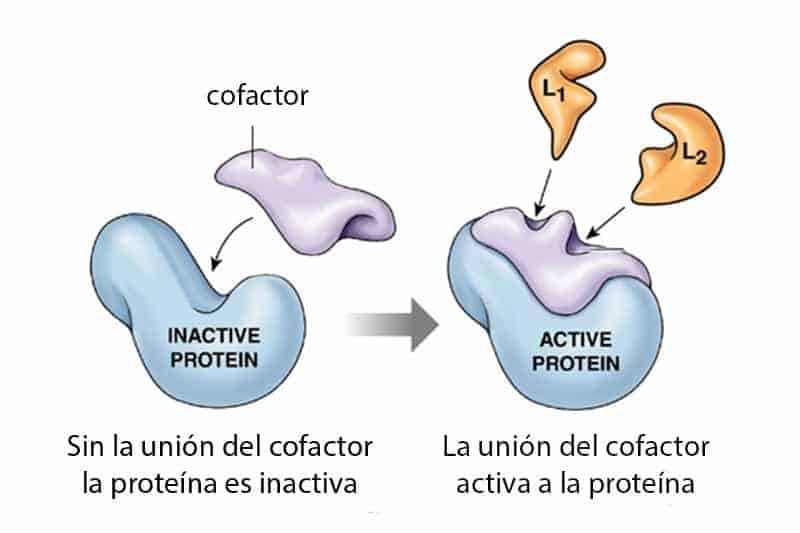 Las enzimas reconocen el sustrato y hacen modificaciones muy concretas, es decir, rompen o forman nuevos enlaces, separan o unen partes de la molécula, modifican la estructura, etc. Hay veces que se necesitan cofactores. Los cofactores son sustancias de naturaleza no proteica, necesarios para que se lleve a cabo la reacción. Cuando son de naturaleza orgánica, se denominas coenzimas. Las coenzimas son componentes adicionales con carácter vitamínico necesarios para que ciertas enzimas actúen con normalidad. (Imagen de la izquierda, curiosoando, dominio público).
Las enzimas reconocen el sustrato y hacen modificaciones muy concretas, es decir, rompen o forman nuevos enlaces, separan o unen partes de la molécula, modifican la estructura, etc. Hay veces que se necesitan cofactores. Los cofactores son sustancias de naturaleza no proteica, necesarios para que se lleve a cabo la reacción. Cuando son de naturaleza orgánica, se denominas coenzimas. Las coenzimas son componentes adicionales con carácter vitamínico necesarios para que ciertas enzimas actúen con normalidad. (Imagen de la izquierda, curiosoando, dominio público).
Normalmente, todas estas acciones se hacen dentro de las células, aunque hay algunos tipos de enzimas en los que no es necesario.
 Factores ambientales
Factores ambientales
Hay factores ambientales que afectan la velocidad de las reacciones, como la temperatura y el pH. Sin un pH óptimo, la velocidad de la reacción baja considerablemente, ya que las enzimas se desnaturalizan. Lo mismo ocurre con la temperatura. Las reacciones químicas dependen de ella, y si baja la temperatura, baja la velocidad de la reacción. (Imagen de la izquierda, bionova, dominio público).
Regulación de la actividad enzimática
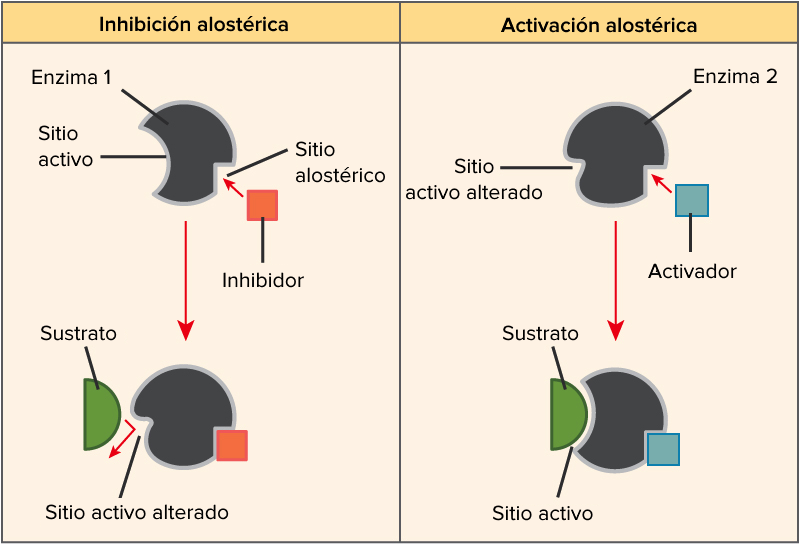 Las enzimas pueden ser reguladas por otras moléculas. Pueden alterar la actividad de la enzima para que se reduzca (inhibidores) o aumente (activadoras). Estas moléculas no se unen permanentemente a las enzimas, sino que en muchos casos son reversibles.
Las enzimas pueden ser reguladas por otras moléculas. Pueden alterar la actividad de la enzima para que se reduzca (inhibidores) o aumente (activadoras). Estas moléculas no se unen permanentemente a las enzimas, sino que en muchos casos son reversibles.
Cuando la molécula se une a la enzima en un sitio distinto al centro activo, se denomina regulación alostérica. Estas producen un ajuste leve a la actividad enzimática que se ejerce en el interior de las células. (Imagen de la derecha, khana academy, dominio público).
Clasificación de las enzimas
Hay muchos tipos de enzimas, divididos según la naturaleza de la reacción y la reacción específica que catalizan.
1. Oxidorreductasas: Son enzimas que catalizan reacciones de óxido-reducción, es decir, reacciones en las que se transfieren átomos de Hidrógeno de un lado a otro. También se da cuando se incorporan átomos de Oxígeno en el sustrato. Ejemplo: Deshidrogenasa.
2. Transferasas: Son enzimas que catalizan reacciones de un grupo químico siendo un par electrónico. Es decir, se transfieren dos átomos de un grupo químico diferente al Hidrógeno. Ejemplo: Glucoquinasa.
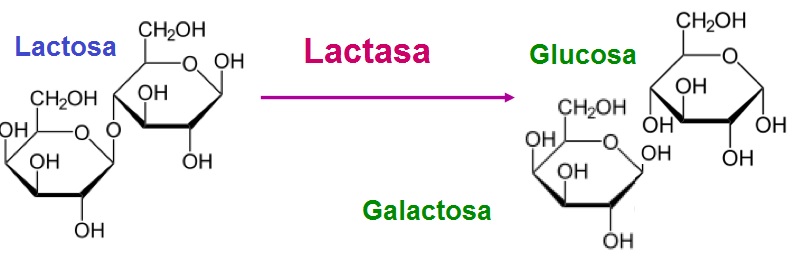
3. Hidrolasas: Son enzimas que catalizan reacciones de hidrólisis. Ejemplo: Lactasa. (Imagen de abajo, Centro Salud Nutricional, dominio público).
4. Liasas: Son enzimas que catalizan reacciones en las que se fracturan o se hacen más fuertes los sustratos. Ejemplo: Descarboxilasa
5. Isomerasas: Estas enzimas catalizan reacciones en las que hay un reagrupamiento dentro de la misma molécula, siendo enzimas monosustrato.
6. Ligasas: Estas enzimas catalizan reacciones en las que se unen como mínimo tres sustratos diferentes mediante hidrólisis. Ejemplo: Enzima privato carboxilasa.
Bibliografía
- Nico Hill, N. H. (s. f.). Enzimas | CANNA España. Recuperado 20-10-17, de https://www.canna.es/enzimas
- Joaquín Ramírez Ramírez, J. R. R., & Marcela Ayala Aceves, M. A. A. (2016). Enzimas: ¿Qué son y cómo funcionan? Recuperado 17 de octubre de 2020, de http://www.revista.unam.mx/vol.15/num12/art91/
- Valenzuela, I. (2018, 2 abril). ¿Cómo funcionan las enzimas? Recuperado 17 de octubre de 2020, de https://www.vix.com/es/btg/curiosidades/6696/como-funcionan-las-enzimas
- biología-geología. (s. f.). El centro activo de las enzimas. Recuperado 17 de octubre de 2020, de https://biologia-geologia.com/biologia2/452_el_centro_activo_de_las_enzimas.html
- Enrique Battaner Arias. (2015). Enzimología. gredos.usal.es. Recuperado de https://gredos.usal.es/bitstream/handle/10366/119453/Enzimologia.pdf?sequence=1&isAllowed=y
- Regulación enzimática (artículo). (2016). Recuperado 17 de octubre de 2020, de https://es.khanacademy.org/science/ap-biology/cellular-energetics/environmental-impacts-on-enzyme-function/a/enzyme-regulation#:%7E:text=Las%20enzimas%20pueden%20ser%20reguladas,una%20enzima%20se%20llaman%20inhibidores
- Federico Granados Martínez, & Victor López Fenoy. (1997). Biología y Geología 1o Bachillerato Ciencias de la Naturaleza y de la Salud. Zaragoza, España: Edelvives.
- Hidrólisis. (s. f.). Recuperado 17 de octubre de 2020, de https://concepto.de/hidrolisis/
- Tipos de catalizadores (artículo) | Cinética. (s. f.). Recuperado 17 de octubre de 2020, de https://es.khanacademy.org/science/ap-chemistry/kinetics-ap/arrhenius-equation-mechanisms-ap/a/types-of-catalysts
- Aminoácidos. (s. f.). Recuperado 17 de octubre de 2020, de https://medlineplus.gov/spanish/ency/article/002222.htm
- Enlace iónico. (s. f.). Recuperado 17 de octubre de 2020, de https://concepto.de/enlace-ionico/
- Diccionario de cáncer del NCI. (s. f.). Recuperado 17 de octubre de 2020, de https://www.cancer.gov/espanol/publicaciones/diccionario/def/ph
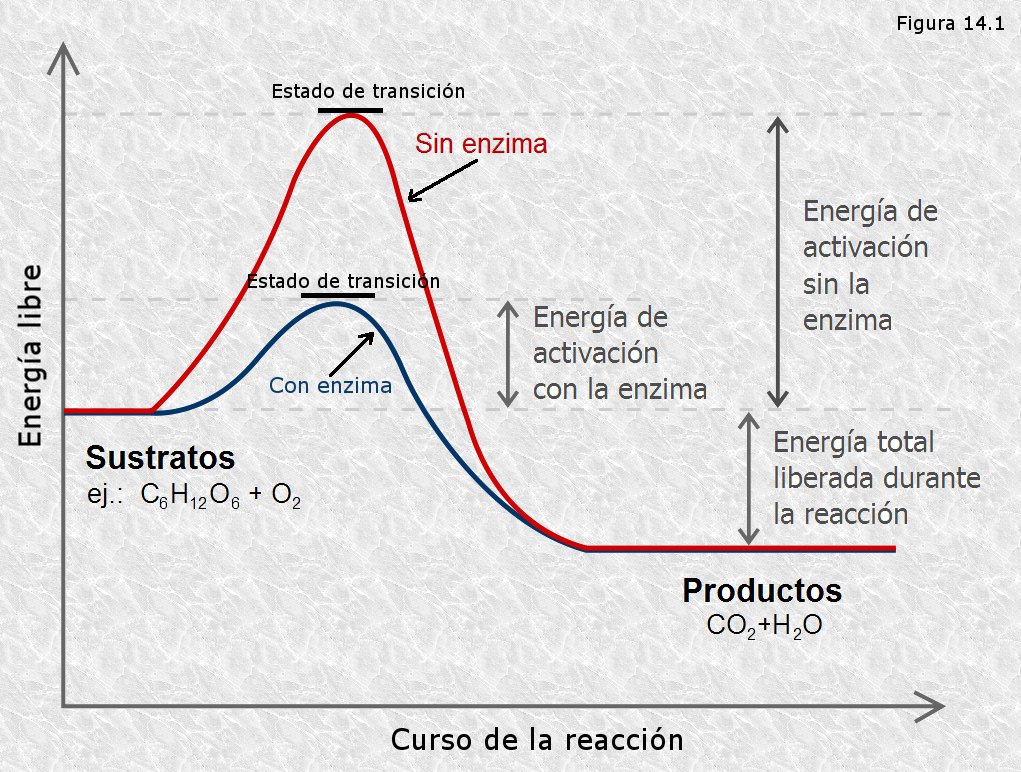
Los catalizadores son sustancias que se añaden en una reacción química para que se aumente la velocidad de reacción, disminuyendo la energía de activación. No se consumen en el proceso.
La hidrólisis es una reacción química en la que el agua se usa como disolvente. Esto quiere decir que las moléculas de agua junto con otras sustancias involucradas, forman nuevos enlaces y nuevas sustancias.
Los aminoácidos son sustancias que forman proteínas. Son uno de los pilares de la vida y se dividen en aminoácidos esenciales, no esenciales y condicionales.
Es un enlace de unión química. Se da en átomos metálicos y no metálicos, dando como resultado una molécula con carga electronegativa llamada ion.
El pH mide el grado de acidez de una sustancia o molécula. Se mide en una escala del 0 al 14. El 7 se considera pH neutro, cuando es menor de 7 es ácido y cuando es mayor de 7 es alcalina. Tener un pH apropiado es importante para el funcionamiento de nuestro cuerpo.