Reacciones Química Orgánica: Compuestos Oxigenados y Nitrogenados
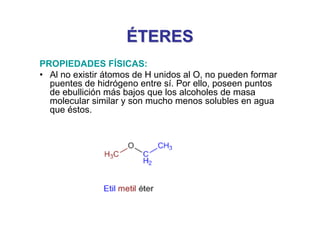
- 1. É ÉTERES TERES PROPIEDADES FÍSICAS: • Al no existir átomos de H unidos al O, no pueden formar puentes de hidrógeno entre sí. Por ello, poseen puntos de ebullición más bajos que los alcoholes de masa molecular similar y son mucho menos solubles en agua que éstos.
- 2. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • CARÁCTER BÁSICO CH3-O-CH3 + HCl -----> CH3-O-H+ Cl- CH3 Cloruro de dimetiloxonio El compuesto formado es un compuesto salino como el catión hidronio y amonio.
- 3. • RUPTURA DE LA UNIÓN C-O CH3-O-CH2-CH3 + HI ----> CH3-OH + CH3-CH2I metanol ioduro de etilo CH3-O-CH2-CH3 + HI ----> CH3-CH2OH + CH3I etanol ioduro de metilo
- 4. • OXIDACIÓN CH3-O-CH2-CH3 + O2-----> CH3-CHO + HCHO + H2O etanal metanal
- 5. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • DESHIDRATACIÓN DE ALCOHOLES Cuando los alcoholes son iguales se obtienen éter simétricos.
- 6. • SÍNTESIS DE WILLIAMSON: Tiene lugar entre un halogenuro de alquilo y un alcóxido. metóxido de sodio éter metílico
- 7. ALCOHOLES ALCOHOLES • Son compuestos orgánicos que contienen un grupo hidroxilo, unido a un carbono que puede formar parte de un compuesto alifático o aromático.
- 8. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • Las propiedades físicas de los alcoholes están relacionados con el grupo -OH, que es muy polar y es capaz de establecer puentes de hidrógeno con sus moléculas compañeras, con otras moléculas neutras, y con aniones. • Esto hace que el punto de ebullición de los alcoholes sea mucho más elevado que los de otros hidrocarburos con igual peso molecular. • El comportamiento de los alcoholes con respecto a su solubilidad también refleja su tendencia a formar puentes de hidrógeno.
- 10. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • FORMACIÓN DE ALCÓXIDOS • Los alcoholes son ácidos débiles. Son ligeramente más débiles que el agua, pero más fuertes que los alquinos terminales, el amoníaco y los alcanos. • La base conjugada del alcohol se denomina ión alcóxido, y es más fuerte como base que el hidroxilo
- 11. • REACCIONES DE SUSTITUCIÓN DEL GRUPO HIDROXILO
- 12. • REACCIONES DE OXIDACIÓN – ALCOHOLES PRIMARIOS • Oxidación suave • Si la oxidación continúa
- 16. • ALCOHOLES TERCIARIOS • No puede ser oxidado. • Para hacerlo se puede recurrir a la utilización de un agente ácido para deshidratarlo a un alqueno, y luego oxidar este a una cetona. • La oxidación enérgica destruye la molécula.
- 17. • COMBUSTIÓN CH3CH2OH + 3O2 ----->2CO2 + 3H2O + calor
- 18. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • HIDRÓLISIS DE HALOGENUROS DE ALQUILO
- 19. • HIDRATACIÓN DE ALQUENOS CH2=CH2 + H2SO4 ---->CH3CH2-SO4H sulfato ácido de etilo CH3CH2-SO4H + H2O ----> CH3CH2OH + H2SO4 etanol
- 20. • REDUCCIÓN DE ALDEHÍDOS Y CETONAS
- 21. FENOLES FENOLES • Se trata de aquellos compuestos que tienen el grupo hidroxilo unido directamente a un anillo aromático.
- 22. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • Se caracterizan por ser líquidos o sólidos de bajo punto de fusión. • Con puntos de ebullición elevados debido a la capacidad para establecer puentes de hidrógeno. • El fenol es algo soluble en agua, pero la mayor parte se caracteriza por ser insoluble.
- 23. PROPIEDADES QUIMICAS PROPIEDADES QUIMICAS • FORMACIÓN DE SALES Fenóxido de sodio
- 24. • FORMACIÓN DE ÉTERES (SINTESIS DE WILLIAMSON) + ICH3 -----> + NaI fenil metil éter
- 25. • FORMACIÓN DE ÉSTERES + CH3COOH ----> + H2O acetato de fenilo
- 26. • BROMACIÓN
- 27. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • HIDRÓLISIS DE HALOGENUROS DE ARILO Fenóxido de sodio
- 28. • POR HIDRÓLISIS DEL ÁCIDO BENCENOSULFÓNICO H2SO4
- 29. ALDEH ALDEHÍ ÍDOS Y CETONAS DOS Y CETONAS • Ambos compuestos se caracterizan por presentar el grupo carbonilo. En los aldehídos este grupo se encuentra en el carbono primario y en las cetonas se halla en un carbono secundario
- 30. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • Son líquidos a temperatura ambiente (excepto el metanal que es un gas). • Sus puntos de ebullición superan a los de los hidrocarburos de masa molecular similar. • Los primeros términos, por la polaridad del grupo carbonilo, son muy solubles en agua.
- 31. PROPIEDADES QUÍMICAS • REACCIONES DE ADICIÓN Por ejemplo la adición del ácido cianhídrico aldehído
- 33. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIONES DE REDUCCIÓN cetona aldehído Alcohol primario Alcohol secundario
- 34. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIONES DE OXIDACIÓN • Los agentes oxidantes suaves oxidan los aldehídos pero no a las cetonas. • Este diferente comportamiento frente a la oxidación permite distinguirlos. • REACCIÓN DE TOLLENS • El reactivo de Tollens se obtiene al mezclar nitrato de plata con amoníaco, ambos en disolución acuosa. • El reactivo oxida los aldehídos a ácidos carboxílicos y al hacerlo, la plata Ag+ se reduce a Ag° . En determinadas condiciones, l a plata se deposita sobre las paredes del tubo de ensayo, formando un espejo.
- 35. Precipita plata metálica en forma de espejo Tollens Bernhard
- 36. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIONES DE OXIDACIÓN • REACCIÓN DE FEHLING • El licor de Fehling esta constituído por una solución de CuSO4 y por otra solución de NaOH y tartrato doble de sodio y potasio en agua.
- 37. • El hidróxido cúprico no precipita, pues con el tartrato doble de sodio y potasio forma un complejo soluble de color azul intenso. • Añadiendo el licor de Fehling a un aldehído y sometiendo el conjunto al calor, el hidróxido cúprico es reducido, el aldehído se transforma en ácido y precipita óxido cuproso de color rojo ladrillo. Precipita óxido cuproso de color rojo ladrillo. Fehling, Hermann von
- 39. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • OXIDACIÓN DE ALCOHOLES • (Idem alcoholes)
- 41. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • HIDRATACIÓN DE ALQUINOS
- 42. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • ACILACIÓN DE FRIEDEL-CRAFTS
- 44. Á ÁCIDOS CARBOX CIDOS CARBOXÍ ÍLICOS LICOS • Los ácidos presentan el grupo funcional carboxilo unido a un hidrógeno, a un grupo arilo o alquilo.
- 45. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • Los primeros términos, hasta el ácido decanoico, son líquidos; los demás son sólidos a temperatura ambiente. • Sus puntos de ebullición son relativamente altos por los puentes de hidrógeno. Se eleva al aumentar el número de átomos de carbono en la cadena. • Dado a la polaridad del grupo hidroxilo, los primeros términos son muy solubles en agua.
- 46. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • SUSTITUCIÓN DEL HIDRÓGENO ACIDICO: FORMACIÓN DE SALES. • En solución acuosa ceden un protón y se convierten en su base conjugada, por lo tanto son capaces de reaccionar con hidróxidos y formar sales, y con un gran número de metales liberando hidrógeno.
- 47. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIONES CON LOS HIDRÓXIDOS.
- 48. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • ACCIÓN SOBRE LOS METALES
- 49. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • FORMACIÓN DE HALOGENUROS DE ÁCIDOS O DE ACILO
- 50. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • FORMACIÓN DE ANHÍDRIDOS
- 51. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • FORMACIÓN DE ÉSTERES
- 52. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • FORMACIÓN DE AMIDAS
- 53. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REDUCCIÓN
- 54. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • OXIDACIÓN DE ALCOHOLES Y ALDEHÍDOS
- 55. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • HIDRÓLISIS DE NITRILOS CH3-CN + 3 H2O ----> CH2-COOH + NH4OH acetonitrilo o etanonitrilo
- 56. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • CARBONATACIÓN DEL REACTIVO DE GRIGNARD CH3-Mg-Cl ------------> CH3-COOH + MgCl2 CLORURO DE ETILMAGNESIO CO2 H+
- 57. HALOGENUROS DE ACILO HALOGENUROS DE ACILO
- 58. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • La presencia del grupo carbonilo confiere polaridad a los derivados de ácidos. • Son compuestos que poseen puntos de ebullición similares a los de los aldehídos y cetonas de masa molecular comparable. • Tienen olores fuertes e irritantes.
- 59. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIONES DE HIDRÓLISIS CH3-CO-Cl + H2O --- -> CH3-COOH + HCl
- 60. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • AMONÓLISIS CH3-CO-Cl + 2 NH3 ----> 2 CH3-CO-NH2 + NH4Cl ETANAMIDA
- 61. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • ALCOHÓLISIS CH3-CO-Cl + CH3-CH2OH ---->CH3-COO-CH2-CH3 + HCl ETANOATO DE ETILO
- 62. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • FORMACIÓN DE HALOGENUROS DE ÁCIDOS O DE ACILO
- 64. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • También se caracterizan por ser compuestos polares. Poseen puntos de ebullición comparables a los de aldehídos y cetonas.
- 65. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIONES DE HIDRÓLISIS CH3-CO.O.CO-CH3 + H2O ----2 CH3-COOH
- 66. • AMONÓLISIS CH3-CO.O.CO-CH3 + 2 NH3 --- CH3-CO-NH2 + NH4CH3COO ETANAMIDA ETANOATO DE AMONIO
- 67. • ALCOHÓLISIS: Transesterificación CH3-CO.O.CO-CH3 + CH3-OH ----- CH3-COO-CH3 + CH3-COOH
- 68. M MÉ ÉTODO DE OBTENCI TODO DE OBTENCIÓ ÓN N • FORMACIÓN DE ANHÍDRIDOS
- 69. É ÉSTERES STERES PROPIEDADES FÍSICAS: • Son líquidos o sólidos. • Los más volátiles tienen olores agradables y muy característicos, por lo que se suelen utilizar en la preparación de perfumes.
- 70. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIONES DE HIDRÓLISIS CH3-COO-CH3 + H2O ---> CH3-COOH + CH3OH ETANOATO DE METILO AC. ACÉTICO METANOL CH3-COO-CH3 + H2O -> NaCH3-COO + CH3-OH ETANOATO DE METILO ACETATO DE SODIO METANOL H+ NaOH
- 71. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • AMONÓLISIS CH3-COO-CH3 + NH3---> CH3-CONH2 + CH3OH ETANOATO DE METILO ACETAMIDA METANOL H+
- 72. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • ALCOHÓLISIS CH3-COO-CH3 + CH2-CH2-OH---> CH3-COO-CH2-CH3 + CH3OH ETANOATO DE METILO ETANOL ACETATO DE ETILO METANOL
- 73. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • A PARTIR DE UN ÁCIDO Y UN ALCOHOL
- 74. • A PARTIR DE UN ANHÍDRIDO Y UN ALCOHOL (ALCOHÓLISIS): CH3-CO.O.CO-CH3 + CH3-OH ----- CH3-COO-CH3 + CH3-COOH
- 75. • A PARTIR DE CLORURO DE ÁCIDO Y UN ALCOHOL (ALCOHÓLISIS) CH3-CO-Cl + CH3-CH2OH ---->CH3-COO-CH2-CH3 + HCl ETANOATO DE ETILO
- 76. AMIDAS AMIDAS
- 77. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • La metanamida es líquida. • Todas las demás amidas sencillas son sólidas a temperatura ambiente. • Como el grupo amida es polar son bastante solubles en agua. • Tienen puntos de ebullición altos por su capacidad de establecer uniones puente de hidrógeno.
- 78. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • HIDRÓLISIS CH3-CO-NH2 + H2O ----> CH3-COOH + (NH4)2SO4 acetamida H2SO4 ÁCIDA
- 79. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • HIDRÓLISIS CH3-CO-NH2 + H2O ----> CH3-COONa + NH3 acetamida NaOH ALCALINA
- 80. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • DESHIDRATACIÓN CH3-CO-NH2 ----> CH3-CN + H2O ETANONITRILO P2O5
- 81. PROPIEDADES QU PROPIEDADES QUÍ ÍMICAS MICAS • REACCIÓN CON ÁCIDO NITROSO CH3-CO-NH2 + HNO2 ----> CH3-COOH + H2O + N2 ACETAMIDA ÁCIDO ETANOICO Permite la identificación de amidas primarias VOLÁTIL
- 82. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • A PARTIR DE HALOGENUROS DE ÁCIDOS Y AMONÍACO SE SUSTITUYE EL GRUPO HIDROXILO
- 83. • A PARTIR DE ANHÍDRIDOS Y AMONÍACO CH3-CO.O.CO-CH3 + 2 NH3 --- CH3-CO-NH2 + NH4CH3COO ETANOATO DE AMONIO ETANAMIDA AMONÓLISIS
- 84. • POR CALENTAMIENTO DE SALES DE AMONIO DE ÁCIDOS CARBOXÍLICOS NH4CH3-COO -----> CH3-CONH2 + H2O ACETATO DE AMONIO ACETAMIDA o ETANAMIDA
- 85. AMINAS AMINAS • Son compuestos orgánicos nitrogenados que pueden considerarse derivados del amoníaco por sustitución de uno o más hidrógenos por un grupo alquílico o un anillo aromático.
- 86. PROPIEDADES F PROPIEDADES FÍ ÍSICAS SICAS • Las más sencillas son gaseosas y a medida que aumenta la masa molecular son líquidas y, después sólidas. • Como pueden establecer puentes hidrógeno, las aminas primarias son más solubles en agua que las terciarias.
- 87. PROPIEDADES QUIMICAS PROPIEDADES QUIMICAS • CARÁCTER BÁSICO CH3-NH2 + H2O ---> [CH3-NH3]+OH- El comportamiento químico se debe a la presencia de 1 par de electrones NO compartidos CARÁCTER BÁSICO Reacción con agua metilamina Hidróxido de metilamonio
- 88. PROPIEDADES QUIMICAS PROPIEDADES QUIMICAS • CARÁCTER BÁSICO CH3-NH2 + HCl ---> [CH3-NH3]+Cl- El comportamiento químico se debe a la presencia de 1 par de electrones NO compartidos CARÁCTER BÁSICO Reacción con ácidos metilamina Cloruro de metilamonio
- 89. PROPIEDADES QUIMICAS PROPIEDADES QUIMICAS • REACCIÓN CON ÁCIDO NITROSO CH3-NH2 + HNO2 ---> CH3-OH + H2O + N2 AMINA PRIMARIA metilamina METANOL VOLÁTIL
- 90. PROPIEDADES QUIMICAS PROPIEDADES QUIMICAS • REACCIÓN CON ÁCIDO NITROSO (CH3)2-NH2 + HNO2 ---> (CH3)2N-N=O + H2O AMINA SECUNDARIA dimetilamina dimetilnitrosamina PRECIPITADO AMARILLO
- 91. PROPIEDADES QUIMICAS PROPIEDADES QUIMICAS • REACCIÓN CON ÁCIDO NITROSO AMINA TERCIARIA NO REACCIONAN
- 92. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • MÉTODO DE HOFFMAN CH3-CH2I + NH3 ----> CH3-CH2-NH2 + HI Ioduro de etilo etilamina
- 93. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • MÉTODO DE DOW C6H5-Cl+ NH3 ----> C6H5-NH2 + HCl clorobenceno aminobenceno anilina
- 94. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • REDUCCIÓN DE NITRILOS CH3-CH2-CH2-CN ---> CH3-CH2-CH2-NH2 propanonitrilo propilamina H2, Ni
- 95. M MÉ ÉTODOS DE OBTENCI TODOS DE OBTENCIÓ ÓN N • REDUCCIÓN DEL GRUPO NITRO C6H5-NO2 ---> C6H5-NH2 nitrobenceno aminobenceno H2, Ni anilina
